Forma de eliberare a unei substanțe medicamentoase determină în mare măsură calea sa de administrare în organism. După ce medicamentul intră în organism, două procese încep simultan:
Schimbarea concentrației de droguri în timp. Aceste procese sunt descrise cantitativ prin farmacocinetică.
Interacțiunea unei substanțe medicinale cu țintele moleculare de acțiune în organele și țesuturile corpului, care determină efectul terapeutic și reacțiile adverse ale medicamentului. Aceste probleme sunt studiate de farmacodinamică.
- Clauzele 1-6 sunt destinate părinților și îngrijitorilor.
- Acesta din urmă este un paragraf special care ar trebui citit de un copil sau adolescent.
Direcții de utilizare a Ritalin?
Ritalin este utilizat pentru a trata „tulburarea de hiperactivitate cu deficit de atenție”. Este utilizat numai după utilizarea altor tratamente care nu necesită utilizarea de medicamente, cum ar fi terapia de întreținere și terapia comportamentală. Este utilizat la copii și adolescenți cu vârste cuprinse între 6 și 18 ani. . Nu se știe dacă Ritalin este sigur sau eficient în aceste populații de pacienți.
Relația dintre farmacocinetică și farmacodinamică este prezentată schematic în figura 1.4. Ambele procese joacă un rol important în mecanismele de acțiune ale medicamentelor, fără ele, dezvoltarea unui efect terapeutic este imposibilă. În condiții reale, nu există o distincție clară între procesele farmacocinetice și farmacodinamice. Încălcarea oricărei componente duce la o modificare a concentrației medicamentului la locul de acțiune și, în consecință, la o scădere a eficacității terapiei sau la o creștere a probabilității de reacții adverse.
Ritalina îmbunătățește activitatea anumitor zone ale creierului care sunt mai puțin active. Medicamentele pot ajuta la îmbunătățirea atenției, a concentrării și la reducerea comportamentului impulsiv. Medicamentul este furnizat ca parte a unui program cuprinzător de tratament, care include de obicei.
Terapie psihologică, terapie educativă și terapie socială. . Este prescris numai de medicii care au experiență cu tulburări de comportament la copii sau adolescenți. Este greu să stai și să te concentrezi. . Nu este vina lor dacă nu o pot face.
Luând metilfenidat cu alcool
Descrierea aspectului Ritalinului și conținutul pachetului
Comprimatele Ritalin sunt disponibile într-o doză de: 10 mg. Nu toate pachetele pot fi vândute. Această informație a fost pregătită pentru a afla caracteristicile de bază ale medicamentului dvs. numit Ritalin. Dacă nu vă place să citiți, cineva ca mama, tata sau persoana care are grijă de dvs. le poate citi și răspunde la orice întrebare.Tabelul 1.7
Concentrația substanței medicamentoase în plasma sanguină și locul de acțiune, precum și dezvoltarea de efecte terapeutice și reacții adverse sunt determinate de regimul de dozare a substanței medicamentoase.
Doza - cantitatea de medicament pe doză. Alocați o singură doză, zilnic și curs. În doze unice, medicamentele sunt de obicei prescrise pentru intervenția de urgență în funcțiile vitale ale organismului. Acțiunea acestor medicamente se manifestă de obicei destul de repede. În doze zilnice, medicamentele sunt de obicei prescrise cu efect cumulativ (cumulativ). În acest caz, doza zilnică poate fi împărțită în mai multe doze. În doze, desigur, sunt prescrise medicamente cu efect terapeutic întârziat. Pentru unele medicamente de acest tip, schemele de administrare au fost selectate empiric care determină cantitatea de substanță medicamentoasă care trebuie administrată într-o zi sau alta a terapiei.
Acest lucru vă poate ajuta să citiți bucăți mici simultan. În timp ce luați acest medicament. Dacă luați acest medicament de mai multe ori pe zi, se poate întâmpla că trebuie să vă amintiți că îl luați la școală. Mama ta, tatăl tău sau o persoană îngrijitoare va trebui să verifice care sunt regulile școlii. Nu bea alcool. Alcoolul poate înrăutăți efectele secundare ale acestui medicament. Fetele trebuie să-și informeze imediat medicul dacă credeți că au o sarcină în desfășurare. Nu știm cum afectează acest lucru medicamentul la un copil nenăscut. Dacă aveți activitate sexuală, discutați cu medicul dumneavoastră despre metodele de control al nașterii. Acest lucru se poate întâmpla în timpul vacanțelor școlare. . Unii oameni nu pot lua acest medicament.
O metodă experimentală este utilizată de obicei pentru a determina dozele de medicamente și pentru a evalua siguranța acestora. Cu ajutorul său, animalele experimentale determină dozele eficiente, toxice și letale în practica experimentală.
Prin eficiență se înțelege o doză care determină un anumit efect farmacologic, de exemplu, antihipertensiv, antiinflamator. Toxic este o doză care duce la dezvoltarea de complicații toxice. Letal - doza care duce la moartea animalelor experimentale. Aceste doze sunt denumite în mod obișnuit ED (doză eficientă), TD (doză toxică) și LD (doză letală).
Nu puteți lua acest medicament dacă. Ai o afecțiune cardiacă, te simți foarte nefericit, deprimat sau ai o tulburare psihică. Unii oameni ar trebui să discute cu medicul lor înainte de a lua acest medicament. Dacă ar trebui să discutați cu medicul dumneavoastră dacă
Suferiți de epilepsie că sunteți gravidă sau alăptați în timp ce luați alte medicamente - medicul trebuie să știe toate medicamentele pe care le luați. Cum iau medicamente?
- Înghițiți medicamentul cu apă.
- Medicul dumneavoastră vă va spune de câte ori pe zi trebuie să luați medicamentul.
- Nu încetați să luați medicamentul înainte de a vorbi cu medicul dumneavoastră.
Cel mai adesea, EDP ED50, ED99, TDP TD50, TD99, LDJ, LD50 și LD99 sunt determinate, adică dozele care au determinat efectul (de exemplu, moartea) în 1; 50 și 99% din animalele studiate. Deci, ED1 caracterizează doza minimă care poate avea un efect farmacologic, ED50 - doza care determină efectul la jumătate din animalele studiate, ED99 - doza care provoacă efectul la aproape toate animalele.
Efectele secundare sunt lucruri nedorite care pot apărea atunci când luați un medicament. Dacă se întâmplă acest lucru, discutați imediat cu un adult despre cineva în care aveți încredere, care vă poate spune medicul. Principalul lucru care vi se poate întâmpla. Fii foarte deprimat și nefericit sau dorește să ai durere. Să fii într-o dispoziție diferită decât de obicei nu este capabil să adormi. Erupțiile pielii, vânătăile care apar ușor, rămân fără viață. Medicina te poate face să te simți somnoros. Dacă vă simțiți somnolent, este important să nu vă implicați în sporturi în aer liber, cum ar fi mersul pe bicicletă sau mersul pe bicicletă, înotul sau cățărarea în copaci, v-ați putea face rău pe voi și pe alții, inima vă bate mai repede decât de obicei.
- Greață, vărsături sau dureri abdominale.
- Acest lucru se poate întâmpla numai atunci când începeți să luați medicamentul.
- Este mai bine să luați medicamente cu mâncare.
- Simțiți-vă emoționat sau nervos.
- Amețeli sau dureri de cap.
Trebuie menționat că, pentru aceeași substanță medicamentoasă, doza eficientă poate varia în funcție de efectul dorit. Deci, pentru un adult, o doză eficientă de acid acetilsalicilic ca agent antitrombotic este de 0,075-0,5 g / zi, ca agent antireumatic - 3 g / zi.
Nu uitați să păstrați medicamentul într-un loc sigur, astfel încât nimeni altcineva să nu-l poată lua, în special frații și surorile mai mici. Acest medicament are o importanță deosebită pentru dumneavoastră - nu lăsați pe altcineva să-l ia. Dacă uitați să luați medicamentul, nu luați două comprimate data viitoare, ci luați doar una ca de obicei. Dacă luați prea mult medicament, spuneți-i mamei, tatălui sau persoanei care îi pasă imediat. Este important să nu luați prea mult medicament, altfel vă veți îmbolnăvi. Nu încetați să luați medicamentul până când medicul nu vă spune că puteți face acest lucru. Acest medicament vă poate ajuta, dar poate răni pe altcineva. . Mama, tata, îngrijitorul, medicul sau asistenta te pot ajuta.
Rețineți că LD este determinat doar la animale. Pentru o persoană, valorile ED sunt determinate și pentru un număr de medicamente, valorile TD. Cu cât este mai lung intervalul dintre ED50 și TD50, cu atât este mai sigură utilizarea acestuia:
Dacă ED99
Dacă ED1
Dacă ED1\u003e TD1, atunci medicamentul este toxic.
Deci, este considerat relativ sigur
Utilizarea AINS, diuretice, glicozide cardiace, etc. Utilizarea medicamentelor anticanceroase, antipsihotice și altele este aproape întotdeauna asociată cu riscul de complicații toxice (vezi tabelul 1.7).
Conținut publicat în ianuarie Informațiile nu pot fi actualizate. Disclaimer și informații utile. O listă completă de excipienți este furnizată în secțiune. Utilizarea prelungită a copiilor și adolescenților. Siguranța și eficacitatea utilizării pe termen lung a metilfenidatului nu au fost evaluate în mod sistematic folosind studii controlate. Tratamentul cu metilfenidat nu trebuie și nu trebuie să continue la nesfârșit. De obicei, tratamentul cu metilfenidat este întrerupt în timpul sau după pubertate.
Tulburările mintale de verificat sunt enumerate mai jos și includ ticuri motorii sau verbale, comportament agresiv sau ostil, agitație, anxietate, depresie, psihoză, manie, delir, iritabilitate, lipsă de spontaneitate, introvertire și încăpățânare excesivă.
Experimentele pe animale nu dezvăluie toate reacțiile terapeutice și adverse posibile. Acest lucru este valabil mai ales în ceea ce privește efectele cumulate și efectele consumului prelungit de medicamente. În aceste condiții, este, de asemenea, dificil să se determine efectele teratogene și mutagene reale. Prin urmare, după testarea substanțelor medicinale noi la animale, acestea sunt examinate la om - și numai atunci sunt permise pentru utilizare.
Se recomandă oprirea administrării de metilfenidat cel puțin o dată pe an pentru a evalua starea copilului. Îmbunătățirea poate persista chiar și atunci când medicamentul este suspendat temporar sau întrerupt definitiv. Siguranța și eficacitatea produsului nu au fost stabilite pentru pacienții din această grupă de vârstă.
Metilfenidatul nu este recomandat pentru utilizare la pacienții vârstnici. Siguranța și eficacitatea nu au fost stabilite pentru pacienții din această grupă de vârstă. Utilizați la copii sub 6 ani. Metilfenidatul nu este recomandat pentru utilizare la copii sub 6 ani. Siguranța și eficacitatea nu au fost stabilite pentru pacienții din această grupă de vârstă.
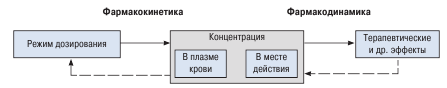
Schema 1.4.
Când se studiază efectele medicamentelor asupra voluntarilor sănătoși, se determină dozele terapeutice minime și minime. Doza terapeutică minimă (analog ED1) este determinată de cantitatea minimă de substanță medicamentoasă care trebuie introdusă pentru a obține un efect terapeutic. Doza toxică minimă (analog TD1) este determinată de cantitatea minimă de substanță medicamentoasă la care începe dezvoltarea efectelor nedorite, secundare sau toxice. Intervalul dintre doza minimă toxică și cea terapeutică se numește interval terapeutic. Cu cât este mai largă gama terapeutică, cu atât este mai mică probabilitatea complicațiilor atunci când utilizați acest medicament. Doza terapeutică minimă și minimă toxică a unei substanțe medicamentoase este determinată în mare măsură de introducerea unei substanțe medicamentoase în organism. Prin urmare, optimizarea terapiei farmacologice poate fi redusă la menținerea concentrației de substanță medicamentoasă într-un anumit țesut în intervalul terapeutic. Acest lucru va permite obținerea unui efect terapeutic fără dezvoltarea de efecte secundare. Întrucât în \u200b\u200bmajoritatea cazurilor nu este posibilă determinarea concentrației unei substanțe medicamentoase la locul acțiunii sale (la punctul de aplicare), concentrația în plasma sanguină este cel mai adesea determinată în practică, deoarece concentrația substanței medicamentoase din plasma sanguină este cea care determină efectul său sistemic: intrarea în organele țintă și dezvoltarea reacții adverse. Prin urmare, optimizarea tratamentului pentru a crește eficacitatea terapiei și a reduce riscul de reacții adverse poate fi redusă la determinarea concentrației unei substanțe medicamentoase în plasma de sânge sau în alte medii biologice ale corpului uman.
În timpul tratamentului cu metilfenidati, pacienții dezvoltă simptome precum palpitații, dureri toracice după exercițiu, leșin inexplicabil, dificultăți de respirație sau alte simptome care sugerează o afecțiune cardiacă; trebuie efectuată o evaluare imediată a inimii.
Nu sunt cunoscute consecințele clinice pe termen scurt și pe termen lung ale acestor efecte asupra sistemului cardiovascular la copii și adolescenți, dar posibilitatea complicațiilor clinice nu poate fi exclusă din cauza influenței datelor studiilor clinice. Prin urmare, trebuie să se facă precauție în tratarea pacienților cu afecțiuni clinice care pot fi afectate de creșterea tensiunii arteriale sau a ritmului cardiac.
Prin urmare, regimul de dozare al substanței medicamentoase trebuie să fie selectat astfel încât concentrația substanței medicamentoase în plasma de sânge să fie în limitele terapeutice. Modelele modificărilor concentrației de medicamente în organism sunt studiate de farmacocinetică. Partea teoretică a acestei științe se bazează pe metode matematice pentru analiza proceselor de schimbare a concentrației de medicamente în organism. Farmacocinetica clinică se bazează pe monitorizarea terapeutică a medicamentului (TLM) - determinarea concentrației de medicamente în țesuturile și fluidele biologice, ceea ce face posibilă selectarea rațională a unui regim individual de dozare pentru un pacient pentru a obține un efect terapeutic maxim și siguranță.
Starea cardiovasculară trebuie monitorizată îndeaproape. Tensiunea arterială și frecvența cardiacă trebuie înregistrate pe o fază grafică la fiecare ajustare a dozei, și apoi cel puțin la fiecare 6 luni. Utilizarea metilfenidatului este contraindicată în prezența anumitor boli cardiovasculare preexistente, cu excepția cazului în care este recomandat de un specialist în cardiologie cu experiență în vârstă de dezvoltare.
Moartea subită și anomalii structurale preexistente sau alte boli grave ale inimii. La copii, unii dintre ei cu anomalii structurale ale inimii sau alte probleme cardiace grave, a fost raportată moartea subită datorită utilizării de stimulanți ai sistemului nervos central pentru utilizare normală în doze pediatrice. Deși unele probleme cardiace grave în sine pot duce la un risc crescut de moarte subită, nu sunt recomandate produse stimulente la copii și adolescenți cu anomalii structurale cunoscute, cardiomiopatie, tulburări severe ale ritmului cardiac sau alte probleme grave ale inimii care le pot face mai vulnerabile Efecte simpatomimetice cauzate de un medicament stimulant al sistemului nervos central.
Farmacocinetica clinică se bazează pe existența unei relații între concentrația de medicament disponibilă pentru determinare (de exemplu, în plasma de sânge sau sânge întreg) și efectele acesteia (terapeutice sau adverse). Pentru multe medicamente, acest lucru este într-adevăr adevărat, dar în unele cazuri nu este posibil să se identifice o astfel de relație. De obicei, concentrația unui medicament în sânge este legată de concentrația sa în țesutul țintă. Farmacocinetica clinică vă permite să cuantificați dependența efectului de doză și să interpretați datele despre dinamica concentrației medicamentului în fluidele biologice. Alegerea și corectarea regimului de tratament ținând cont de legile farmacocinetice permite creșterea eficacității și siguranței tratamentului medicamentos.
Efecte abuzive și efecte cardiovasculare. Utilizarea greșită a stimulanților sistemului nervos central poate fi asociată cu moartea subită și alte efecte secundare cardiovasculare grave. Secțiunea 3 privind afecțiunile cerebrovasculare pentru care este contraindicat tratamentul cu metilfenidat.
Pacienții cu factori de risc suplimentari trebuie monitorizați în mod regulat la fiecare vizită după începerea tratamentului cu metilfenidat pentru a verifica apariția semnelor și simptomelor neurologice. Vasculita cerebrală este o reacție particulară foarte rară la efectele asupra metilfenidatului. Există puține dovezi că un pacient cu risc ridicat poate fi identificat și că debutul inițial al simptomelor poate fi primul semn al unei probleme clinice majore. Un diagnostic precoce bazat pe o rată mare de suspiciune poate permite suspendarea rapidă a metilfenidatului și tratamentul la timp.
Necesitatea modificării dozei pentru anumite afecțiuni fiziologice și patologice se datorează adesea unei modificări în farmacocinetica medicamentului. Cei mai importanți parametri farmacocinetici includ clearance-ul care caracterizează eliminarea medicamentului, volumul de distribuție este volumul aparent în care este conținut medicamentul, timpul de înjumătățire (Tu) este un parametru care caracterizează rata de eliminare a medicamentului din organism, iar biodisponibilitatea este proporția medicamentului administrat în circulația sistemică. . Parametrii mai puțin importanți sunt rata de aspirație și rata de distribuție.
Prin urmare, acest diagnostic trebuie luat în considerare la orice pacient care dezvoltă noi simptome neurologice compatibile cu diagnosticul de ischemie cerebrală în timpul terapiei cu metilfenidat. Aceste simptome pot include dureri de cap severe, amorțeală, slăbiciune, paralizie și o schimbare în coordonare, viziune, vorbire sau memorie.
Tratamentul cu metilfenidat nu este contraindicat la pacienții cu paralizie cerebrală hemiplegică. În cazul simptomelor psihiatrice sau agravării simptomelor psihiatrice preexistente, metilfenidatul nu poate fi administrat decât dacă beneficiile tratamentului depășesc riscurile pentru pacient. Înainte de a începe tratamentul cu ritalină, pacienții trebuie monitorizați pentru prezența tulburărilor mintale în istoricul personal și familial.
Clearance-ul medicamentelor
Acesta este cel mai important parametru farmacocinetic care vă permite să alegeți un regim de doză cu tratament de lungă durată. Pentru a asigura efectul terapeutic necesar și a reduce riscul de reacții adverse, concentrația medie a medicamentului în serul din sânge în stare staționară ar trebui să se încadreze în intervalul terapeutic. Dacă biodisponibilitatea este de 100%, în stare staționară, rata de eliminare a medicamentului este egală cu rata de primire a acestuia.
Rata de sosire \u003d Cl x Media (1.1)
În cazul în care rata de intrare este cantitatea de medicament administrată pe unitate de timp, C1 este clearance-ul total, iar Sredn este concentrația medie a medicamentului în serul din sânge în stare staționară. Dacă se cunoaște concentrația medie necesară a medicamentului în ser, rata de admitere poate fi calculată prin clearance.
Cea mai importantă caracteristică clinică a clearance-ului este că, de regulă, nu depinde de concentrația medicamentului. Cert este că sistemele responsabile de eliminarea majorității medicamentelor (enzimă, transport) nu sunt de obicei saturate, iar rata absolută de eliminare depinde liniar de concentrația medicamentului în ser. Cu alte cuvinte, eliminarea se supune cineticii de prim ordin - proporția medicamentului eliminat pe unitatea de timp este constantă. Dacă sistemele de eliminare sunt saturate, proporția nu este constantă, ci cantitatea de medicament eliminată pe unitatea de timp. În acest caz, eliminarea se supune cineticii de ordin zero, iar clearance-ul depinde de concentrația medicamentului în serul sanguin:?
C1 \u003d Vm / (Km + C), (1,2)
În cazul în care Km este concentrația medicamentului la care rata de eliminare este jumătate din maxim, Vm este rata maximă de eliminare, C este concentrația medicamentului în ser.
Conceptul de clearance-ul unui medicament este similar cu cel al clearance-ului în fiziologia rinichilor. Deci, clearance-ul creatininei este egal cu raportul dintre rata de excreție a creatininei urinare și concentrația de creatinină plasmatică. În general, clearance-ul unui medicament este egal cu raportul dintre rata de eliminare a substanței de către toate organele și concentrația medicamentului în fluidul biologic.
C1 \u003d rata de eliminare / C. (1.3)
Dacă clearance-ul este constant, rata de eliminare este direct proporțională cu concentrația medicamentului. Clearance-ul nu reflectă cantitatea de medicament eliminată, ci volumul de lichid biologic (plasma sanguină sau sângele întreg) care este complet eliminat de această substanță pe unitatea de timp. Acest indicator poate fi calculat pentru plasma de sânge sau sânge întreg, precum și pentru a determina eliberarea medicamentului liber.
Eliminarea medicamentelor este realizată de rinichi, ficat și alte organe. Calculând clearance-ul pentru fiecare organ ca raport al ratei de eliminare de către acest organ la concentrația de medicament (de exemplu, în plasma de sânge) și însumând clearance-ul pentru toate organele, obținem clearance-ul total.
C1poch + C1poch + C1pr \u003d C1, (1.4)
În cazul în care S1poch este clearance renal, S1pech este clearance hepatic, S1pr este clearance pentru alte organe (medicamentele pot fi metabolizate în alte organe, excretate în fecale, transpirație, salivă).
Într-o stare staționară, clearance-ul total poate fi determinat folosind ecuația 1.1. Cu o singură administrare a medicamentului, a cărei biodisponibilitate este de 100%, iar eliminarea se supune cineticii de prim ordin, clearance-ul total poate fi calculat pe baza legii conservării masei și a integrării ecuației 1.3 în timp.
C1 \u003d Doza / ASC. (1.5)
De exemplu. Clearance-ul propranololului (pentru sângele întreg) este de 16 ml / min / kg (1120 ml / min cu o greutate corporală de 70 kg). Medicamentul este eliminat în principal de ficat, adică în 1 min ficatul curăță 1120 ml sânge de propranolol. Clearance-ul nu corespunde întotdeauna cu fluxul plasmatic (sau fluxul de sânge) prin organismul responsabil de eliminare. Dacă medicamentul se leagă de globulele roșii, rata de livrare a acestuia către acest organ este semnificativ mai mare decât se poate presupune pe baza concentrației medicamentului în plasma sanguină. În stare staționară, clearance-ul pentru plasma de sânge și sângele întreg este următorul:
C1n / C1k \u003d Сk / Сn \u003d 1 + Ht x [Се / Сn -1], (1,6)
În cazul în care C1n este clearance-ul pentru plasma sanguină, C1k este clearance-ul pentru sângele întreg, Cn este concentrația medicamentului în plasma sanguină, Ck este concentrația medicamentului în sângele întreg, Ce este concentrația medicamentului în globulele roșii, Ht este hematocritul.
Astfel, clearance-ul pentru sângele întreg este egal cu coeficientul de separare a clearance-ului pentru plasma sanguină prin raportul dintre concentrațiile de medicamente din sângele întreg și plasma sanguină.
distribuire
Volumul distribuției
Acest al doilea parametru farmacocinetic cel mai important caracterizează distribuția medicamentului în organism. Volumul de distribuție (V) este egal cu raportul dintre substanța totală din corp (CCA) și concentrația sa (C) în plasma sanguină sau sânge întreg. Volumul de distribuție nu corespunde adesea cu niciun volum real. Acest volum este necesar pentru o distribuție uniformă a substanței într-o concentrație egală cu concentrația acestei substanțe în plasma sanguină sau sânge întreg.
Vp \u003d CCA / C. (1,7)
Volumul de distribuție reflectă proporția de substanță conținută în spațiul extravascular. La o persoană care cântărește 70 kg, volumul plasmatic din sânge este de 3 l, ccc este de aproximativ 5,5 l, lichidul extracelular este de 12 l, conținutul total de apă din corp este de aproximativ 42 l. Totuși, volumul distribuției multor substanțe medicinale este mult mai mare decât aceste valori. De exemplu, dacă o persoană care cântărește 70 kg conține 500 micrograme de digoxină în corpul său, concentrația sa plasmatică este de 0,75 ng / ml. Împărțind conținutul total de digoxină din organism în funcție de concentrația sa în plasma sanguină, descoperim că volumul de distribuție al digoxinei este de 650 l. Aceasta este de mai mult de 10 ori conținutul total de apă din organism. Cert este că digoxina este distribuită în principal în miocard, mușchi scheletici și țesut adipos, astfel încât conținutul său în plasma sanguină este mic. Volumul de distribuție a medicamentelor care se leagă activ de proteinele plasmatice (dar nu de componentele țesuturilor) corespunde aproximativ volumului plasmei din sânge. Cu toate acestea, unele medicamente sunt conținute în plasmă în principal sub formă legată de albumină, dar au un volum de distribuție mare datorită depunerii în alte țesuturi.
înjumătățire plasmatică prin eliminare
Timpul de înjumătățire (T1 / 2) este timpul în care concentrația unei substanțe din serul din sânge (sau conținutul său total din organism) este redusă la jumătate. În cadrul modelului cu o cameră unică, determinarea T1 / 2 este foarte simplă. Valoarea rezultată este apoi utilizată pentru a calcula doza. Cu toate acestea, pentru multe medicamente, este necesar să se utilizeze un model cu mai multe camere, deoarece dinamica concentrației lor în serul sanguin este descrisă de mai multe funcții exponențiale. În astfel de cazuri, se calculează mai multe valori T1 / 2.
Acum se acceptă în general că Ti depinde de clearance-ul și de volumul distribuției substanței. Într-o stare staționară, relația dintre Ti, clearance și volumul de distribuție a substanței este descrisă aproximativ prin următoarea ecuație:
T1 / 2 "0,693 x Vp / Cl. (1.8)
Garda la sol caracterizează capacitatea organismului de a elimina substanța, prin urmare, cu o scădere a acestui indicator datorită creșterii bolii T1 / 2. Dar acest lucru este valabil numai dacă volumul de distribuție al substanței nu se modifică. De exemplu, odată cu vârsta, T diazepamul crește, dar nu datorită scăderii clearance-ului, ci datorită creșterii volumului de distribuție (Klotzet și colab., 1975). Gradul de legare a unei substanțe la plasmele sanguine și la proteinele țesutului afectează clearance-ul și volumul de distribuție, astfel încât nu este întotdeauna posibilă prezicerea unei modificări a T1 / 2 într-o anumită stare patologică.
Până la T1 / 2 nu este întotdeauna posibilă aprecierea modificării eliminării medicamentului, dar acest indicator vă permite să calculați timpul pentru a ajunge la o stare staționară (la începutul tratamentului, precum și la modificarea dozei sau a frecvenței de administrare). Concentrația substanței medicamentoase în serul din sânge, care este aproximativ 94% din media staționată, se realizează într-un timp egal cu 4 x T1 / 2. În plus, folosind T1 / 2, puteți estima timpul necesar pentru eliminarea completă a substanței din corp și calculați intervalul dintre injecții.
Rata de biodisponibilitate și rata de absorbție
biodisponibilitate
După cum sa menționat mai sus, nu toate medicamentele absorbite intră în circulația sistemică. Cantitatea de medicament care intră în circulația sistemică depinde nu numai de doză, ci și de biodisponibilitate. Acesta din urmă este determinat de gradul de absorbție, precum și de gradul de eliminare la care este expus medicamentul înainte de a intra în circulația sistemică. Pe lângă absorbția incompletă (vezi mai sus), biodisponibilitatea scăzută se poate datora metabolismului intens în intestine sau ficatului sau excreției cu bilă.
Rata de aspirație
De regulă, rata de absorbție nu afectează concentrația medie a medicamentului în serul din sânge în stare staționară, dar poate afecta semnificativ efectele farmacologice. Dacă medicamentul intră rapid în circulația sistemică (de exemplu, prin administrarea intravenoasă a jetului) și este distribuit inițial într-un volum mic, concentrația sa în serul din sânge poate fi destul de mare. Pe măsură ce medicamentul este distribuit în organele și țesuturile mai puțin intens circulate, acesta scade. Dacă medicamentul intră mai lent în circulația sistemică (de exemplu, prin perfuzie intravenoasă), distribuția acestuia începe chiar înainte de administrarea întregii doze. Prin urmare, concentrația maximă în serul sanguin este mai mică și se ajunge mai târziu. Medicamentele cu acțiune lungă asigură o absorbție lentă și uniformă a medicamentelor, reducând fluctuațiile concentrației medicamentului în serul din sânge între administrații. Rata de distribuție a substanței medicamentoase în diferite țesuturi țintă poate fi diferită, prin urmare, cu o modificare a vitezei de administrare, severitatea efectelor terapeutice și a reacțiilor adverse se poate modifica temporar.
Selectarea și ajustarea dozei
Efectul terapeutic cu o singură injecție de medicament apare la ceva timp după introducere, maximul este atins treptat, apoi slăbește și dispare.
Dinamica acestuia corespunde concentrației medicamentului în serul sanguin, care este determinată de caracteristicile farmacologice ale acestuia (absorbție, distribuție, eliminare). Efectul terapeutic apare la atingerea unei concentrații terapeutice și crește pe măsură ce crește. Durata efectului depinde de perioada în care concentrația medicamentului în serul din sânge depășește terapeutic. În mod similar, reacțiile adverse depind de concentrația toxică a medicamentului. În intervalul dintre aceste concentrații (interval terapeutic), medicamentul este eficient, dar nu are reacții adverse. Odată cu administrarea repetată a medicamentului, doza și intervalul dintre administrări sunt selectate astfel încât să obțină efectul terapeutic maxim cu efecte secundare minime. Limita inferioară a intervalului terapeutic, de regulă, este concentrația medicamentului în ser, la care efectul terapeutic este aproximativ jumătate din maxim. Limita superioară corespunde concentrației în care reacțiile adverse apar la cel mult 5-10% dintre pacienți. Concentrația toxică a unor medicamente este mai mică de 2 ori decât concentrația terapeutică. Trebuie amintit despre caracteristicile individuale ale pacienților: unii tolerează bine concentrația medicamentului în serul din sânge care depășește toxic, în timp ce alții au reacții adverse pronunțate atunci când concentrația în serul din sânge rămâne în intervalul terapeutic.
Dacă efectele farmacologice ale medicamentelor sunt ușor de evaluat (de exemplu, prin modificări ale tensiunii arteriale sau a glicemiei), doza poate fi selectată prin încercare și eroare. Pentru a determina măsura în care și cât de des este posibilă modificarea dozei, se aplică reguli empirice care iau în considerare modelele farmacologice de mai sus (de exemplu, doza este modificată cu nu mai mult de 50% și nu mai mult de 3-4 TIs). Dacă nu există toxicitate dependentă de doză, pentru a asigura eficiența maximă și pentru a crește durata medicamentului, îl puteți utiliza într-o doză semnificativ mai mare decât media terapeutică. Deci, de exemplu, se întâmplă cu majoritatea blocantelor p-adrenoreceptor.
Dacă efectele farmacologice sunt dificil de evaluat, medicamentul are o gamă terapeutică restrânsă, un risc ridicat de reacții adverse cu insuficiență de tratament sau medicamentul este utilizat în scopuri profilactice, doza este modificată ușor, observând cu atenție pacienții pentru a identifica reacțiile adverse. Într-un fel sau altul, concentrația medie a medicamentului în stare staționară ar trebui să fie în limitele terapeutice. În cele mai multe cazuri, nu este necesară determinarea concentrației reale a medicamentului în serul din sânge: trebuie doar să știi cum depinde de doza și frecvența de administrare. Cu toate acestea, pentru un număr mic de medicamente, concentrația terapeutică diferă de cea toxică doar printr-un factor de 2-3 (digoxină, teofilină, lidocaină, aminoglicozide, ciclosporine, anticonvulsivante) în stare staționară, în care este eficientă, dar provoacă un minim de reacții adverse. Apoi măsurați concentrația reală a medicamentului și, dacă este necesar, ajustați doza astfel încât concentrația reală să fie cât mai aproape de dorința.
Doza de întreținere
În cele mai multe cazuri, medicamentele sunt administrate fracționat sau sub formă de perfuzie, astfel încât concentrația staționară să se încadreze în intervalul terapeutic. Într-o stare staționară, rata consumului de droguri este egală cu rata de eliminare a acestuia. Substituind concentrația necesară a medicamentului în serul din sânge în ecuație, obținem:
Rata de sosire \u003d Media * C1 / F, (1,9)
Unde F este biodisponibilitatea.
Cunoscând concentrația serică necesară a medicamentului, clearance-ul și biodisponibilitatea acestuia, este posibil să se calculeze doza și frecvența de administrare.
Doza și frecvența de administrare (adică, rata consumului de medicamente) pot fi calculate pe baza ecuației 1.9. Biodisponibilitatea digoxinei este de 0,7.
Rata de intrare \u003d media C, * C1 / F \u003d 1,5 ng / ml * 1,6 / 0,7 ml / min / kg \u003d 3,43 ng / kg / min \u003d 236 ng / min \u003d 236 * 60 * 24 / 1000 μg / zi \u003d 340 μg / zi \u003d 0,34 mg / zi.
În practică, doza este rotunjită la cel mai apropiat standard, de exemplu, la 375 mcg / zi sau la 0,25 mg / zi. În primul caz, concentrația medie în plasma sanguină în stare staționară va fi 1,5 x 375/340 \u003d 1,65 ng / ml, în al doilea - 1,5 x 250/340 \u003d 1,1 ng / ml. ?
Intervalul dintre administrații
Este de dorit ca în intervalul dintre injecții să nu existe fluctuații puternice ale concentrației medicamentului în serul din sânge. Dacă absorbția și distribuția medicamentului s-ar produce instantaneu, mărimea acestor fluctuații ar depinde doar de Ti. Când intervalul dintre administrații este egal cu Ti, concentrația minimă și maximă diferă de 2 ori, ceea ce este destul de acceptabil.
Dacă intervalul terapeutic al medicamentului este suficient de larg, adică în concentrații semnificativ mai mari decât cele terapeutice, este bine tolerat, pot fi prescrise doze maxime. În acest caz, intervalul dintre injecții poate fi mult mai mare decât T, ceea ce este foarte convenabil pentru pacient.
Pentru un medicament cu un interval terapeutic îngust, este deseori necesar să se măsoare concentrațiile maxime și minime ale medicamentului în ser. Concentrația minimă în stare de echilibru (Cmin) a digoxinei este calculată prin următoarea ecuație:
Unde k \u003d 0,693 / Tu, și T este intervalul dintre administrații. Valoarea e-CT reprezintă proporția dozei anterioare rămase în organism la momentul următoarei doze (ținând cont de biodisponibilitate).
O doză de saturație poate fi luată pe cale orală sau administrată intravenos. Pentru a reduce riscul de reacții adverse, acesta este zdrobit. Inițial, se administrează 0,5 mg, după 6-8 ore - încă 0,25 mg, observând cu atenție pacientul. Ultimele 0,25 mg, dacă este necesar, pot fi, de asemenea, împărțite în 2 doze de 0,125 mg și administrate la intervale de 6-8 ore, mai ales dacă este planificat trecerea la administrarea digoxinei într-o doză de întreținere în 24 de ore de la începutul tratamentului.
Selectarea individuală a dozei
Regimul de tratament este determinat pe baza modelelor de absorbție, distribuție și eliminare a medicamentului și a parametrilor farmacocinetici C1, Ur și T1 / 2). Regimurile recomandate sunt de obicei concepute pentru pacientul „mediu”. Pentru multe medicamente, abaterea standard a parametrilor precum F, C1 și Ur este, respectiv, 20; 50 și 30%. Cu alte cuvinte, în 95% din cazuri, concentrația medicamentului în serul din sânge în stare staționară este cuprinsă între 35 și 270%, ceea ce este inacceptabil pentru medicamentele cu un interval terapeutic îngust. Prin urmare, selecția individuală a dozei și a frecvenței de administrare este cea mai importantă condiție pentru eficacitatea tratamentului. Pe baza tiparelor farmacologice descrise mai sus, regimul de tratament este selectat astfel încât să asigure efectul terapeutic necesar și să reducă la minimum riscul de reacții adverse. Dacă este posibil, măsurați concentrația de medicamente în serul din sânge. Pe baza datelor obținute prin tehnici speciale, se corectează doza de medicamente cu un interval terapeutic îngust (de exemplu, glicozide cardiace, medicamente antiaritmice, difenină, teofilină).
Metodele cantitative și calitative de farmacocinetică sunt complexe și costisitoare pentru utilizare obișnuită, ceea ce nu este, de asemenea, justificat în multe cazuri, deoarece există scheme bine stabilite de dozare și corectare a acestora, ținând cont de caracteristicile individuale ale pacienților. Cu toate acestea, în unele cazuri, aceasta necesită monitorizare terapeutică a medicamentelor, care este necesară în următoarele situații, care sunt în primul rând legate (Belousov Yu.B., Gurevich K.G., 2005):
1. Variație individuală semnificativă a parametrilor farmacocinetici ai medicamentelor. De exemplu, există cazuri când efectul terapeutic al medicamentului în plasma de sânge a fost obținut cu o concentrație terapeutică minimă. Astfel, efectele hepatotoxice acute datorate utilizării paracetamolului au fost observate în plasma sanguină, în conformitate cu culoarul terapeutic, și au fost excluși alți factori care ar putea duce la o astfel de complicație (de exemplu, alcoolism).
2. Caracteristicile farmacocineticii la copii și vârstnici. Primii au remarcat variații semnificative în dezvoltarea metabolismului și excreției unei substanțe medicamentoase. La aproape toate persoanele în vârstă, sunt identificate boli care modifică parametrii farmacocinetici ai medicamentelor cunoscute sau necesită terapie complexă, în care pot apărea interacțiuni imprevizibile cu medicamente. În plus, odată cu vârsta, chiar și la persoanele fără boli renale, se observă o scădere a clearance-ului creatininei renale, ceea ce caracterizează o scădere a eficacității sistemului de eliminare a medicamentelor.
3. Gama terapeutică restrânsă a medicamentului, probabilitatea ridicată de a produce reacții adverse chiar și atunci când utilizați concentrații terapeutice minime ale medicamentului.
4. Perioada de sarcină, alăptarea și alte condiții în care este necesară eliminarea completă a riscului de reacții adverse la terapia medicamentoasă sau situațiile în care parametrii farmacocinetici ai medicamentelor se schimbă semnificativ.
5. Farmacocinetica neliniară a medicamentelor, atunci când nu există nicio relație clară între concentrația unei substanțe medicamentoase în sânge și efectul terapeutic. În acest caz, este de obicei postulat că dezvoltarea reacțiilor adverse este asociată cu o modificare a concentrației substanței medicamentoase în plasma sanguină sau în țesutul efector.
6. Bolile care modifică parametrii farmacocinetici ai medicamentelor: insuficiență cardiacă, insuficiență hepatică și renală, boli ale tractului gastro-intestinal.
7. Nevoia de tratament complex, imprevizibilitatea efectelor farmacoterapiei combinate. În acest caz, pacientul trebuie să țină cont de medicamentele fără vânzare, de componentele pe bază de plante, precum și de natura dietei. În general, monitorizarea terapeutică a medicamentului este necesară atunci când\u003e 5 medicamente sunt utilizate simultan, inclusiv forme de dozare topice, vitamine, contraceptive hormonale, medicină tradițională, substanțe homeopate etc. Cu toate acestea, atunci când se prescriu medicamente potențiale sau care au același sistem metabolic, sau în toate cazurile specificate la clauzele 1-6, poate fi necesară monitorizarea terapeutică chiar și atunci când\u003e 2 medicamente sunt utilizate.
prescrierea medicamentelor într-o anumită cantitate (doză) sau într-o anumită concentrare (cu uz local sau inhalator).
Există doze unice (cantitatea de medicament pe doză), doze zilnice (cantitatea de medicament prescrisă pentru o zi în una sau mai multe doze), doze de curs (cantitatea totală a medicamentului pe fiecare tratament). Dacă este necesar, creați rapid la începutul tratamentului o concentrație mare a unei substanțe medicinale în organism, medicamentele sunt prescrise în așa-numitele doze de șoc, care depășesc dozele unice ulterioare.
Dozele în care medicamentul este utilizat în scop terapeutic sau profilactic se numesc terapeutice. Dintre ele, se disting pragul sau acțiunea minimă, dozele terapeutice medii și cele mai mari. Cele mai mari doze terapeutice (unice și zilnice) pentru medicamente toxice și potențiale sunt date în Farmacopeea de Stat a URSS în articole despre medicamente individuale, precum și în două tabele sumare în care cele mai mari doze terapeutice pentru adulți și copii sunt prezentate separat. Pentru copii, aceștia sunt administrați în funcție de vârstă (pentru copiii sub 6 luni, de la 6 luni la 1 an, la 2 ani, la 3-4 ani, 5-6 ani, 7-9 și 10-14 ani). Gama de doze terapeutice, adică. intervalul dintre prag și cele mai mari doze terapeutice este notat prin termenul „lățime terapeutică”. Deoarece dozele de prag sunt rareori utilizate în practică, lățimea terapeutică a medicamentelor este de obicei apreciată prin intervalul dintre dozele terapeutice medii și mai mari. Cu cât este mai mare lățimea terapeutică a medicamentului, cu atât utilizarea sa este mai sigură (riscul mai mic de supradozaj).
Dozele sunt de obicei indicate în grame sau fracții dintr-un gram. Cu o mică lărgime terapeutică de medicamente, ele sunt uneori dozate la 1 kg greutatea corporală (de exemplu, 1 mg / kg) sau pe unitatea de suprafață a corpului (de exemplu, 1 mg / m2). Dozele de substanțe medicinale care depășesc cele mai mari terapeutice sunt desemnate toxice. În aceste doze, medicamentele pot provoca efecte toxice dăunătoare pentru organism. În plus, dozele letale sunt izolate.
Odată cu creșterea dozei de medicament, perioada latentă a acțiunii sale scade de obicei, mărimea și durata efectului cresc.
În practica experimentală, dozele medii eficiente (ED 50), adică doze care determină un anumit efect farmacologic (de exemplu, poziția laterală, pragul crescut al sensibilității la durere etc.) la 50% din animalele experimentale, precum și dozele medii (letale) (LD 50), adică. doze care provoacă moartea a 50% din animalele experimentale pentru o perioadă determinată de timp. Relație - se notează prin termenul „index terapeutic”. Comparând ED50 a două sau mai multe medicamente, se poate judeca activitatea lor relativă (de exemplu, dacă ED50 a medicamentului A este de 2 ori mai mic decât ED 50 al medicamentului B, atunci medicamentul A este de 2 ori mai activ decât medicamentul B). Eficacitatea relativă a substanțelor este evaluată după amploarea efectului farmacologic maxim.
Valoarea dozelor eficiente depinde de biodisponibilitatea medicamentelor și, în consecință, de concentrația acestora din urmă în plasma sanguină. Prin urmare, cea mai precisă selecție de doze eficiente este posibilă, cu condiția să fie stabilită biodisponibilitatea medicamentelor la pacienți specifici.
În aceleași doze ale unei substanțe medicinale, severitatea efectului său terapeutic poate fi diferită, care depinde de diferențele de sensibilitate a organismului la medicamente sub influența mai multor factori (vârstă, sex, starea funcțională a corpului, administrarea repetată a medicamentului, ora administrării acestuia în timpul zilei etc. ). În unele cazuri, modificările sensibilității organismului la medicamente individuale pot fi foarte pronunțate, ceea ce necesită ajustarea adecvată a dozei pentru astfel de medicamente.
Deci, în legătură cu o creștere a sensibilității organismului la medicamente, iar la vârstnici, pacienții cu vârsta peste 60 de ani, medicamente care deprimă omul de știință central (somnifere, antipsihotice, analgezice narcotice, bromuri), glicozide cardiace și diuretice sunt prescrise în doze de 1/2 și alte medicamente toxice și puternice în doze de 2/3 din doze pentru persoanele de vârstă mijlocie. Antibioticele, sulfonamidele și preparatele vitaminice sunt de obicei prescrise persoanelor în vârstă la aceleași doze ca și persoanele de vârstă mijlocie.
